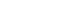மருந்துகளை சந்தைப்படுத்துவதற்கு அதிகாரம் பெற்றுக்கொள்ளுவதற்கான நடைமுறை
படிநிலை 1 - மருந்துகளைப் பதிவுசெய்வதற்காக புதிய தயாரிப்பாளரை அங்கீகரித்தல்
தயாரிப்பு அமைவிடத்திற்கான அங்கீகாரத்திற்காக ஒரு விண்ணப்பத்தைச் சமர்ப்பிக்க வேண்டும். தயாரிப்பாளர் வெளிநாட்டவராக இருந்தால், தயாரிப்பாளரை பிரதிநிதித்துவப்படுத்துவதற்கு உள்ளூர் கம்பெனியொன்றுக்கு அதிகாரம் அளிக்கப்பட்டிருக்க வேண்டும். அத்துடன் அனைத்து விண்ணப்பங்களும் மேற்குறிப்பிட்ட உள்ளூர் முகவர் ஊடாகச் சமர்ப்பிக்கப்படுதல் வேண்டும்.
தயாரிக்கும் அமைவிடம் அங்கீகரிக்கப்பட்ட பின்னர், குறித்த தயாரிப்பாளரால் தயாரிக்கப்படுகின்ற மருந்துகளைப் பதிவுசெய்வதற்காக ஒரு விண்ணப்பம் சமர்ப்பிக்கப்பட வேண்டும்.
படிநிலை 2 - மருந்துகளின் பதிவு
விண்ணப்பத்தின் வகைகள் : அங்கீகாரத்திற்காக விண்ணப்பங்களைச் சமர்ப்பிப்பதற்கு மருந்துகள் பின்வரும் வகைகளாகப் பிரிக்கப்படுகின்றன.
புதிய மூலக்கூறு உள்பொருள்(NME)
இது ஒரு இரசாயன பாதியாகும். இது இலங்கையில் இதற்கு முன்னர் பதிவுசெய்யப்படவில்லை. இதில் செயலூக்கமுள்ள கலவையான உப்பு, ஓர் அமிலம் கலந்த கூட்டுப்பொருள் அல்லது பல பாகங்களைக் கொண்ட முன்னர் அங்கீகரிக்கப்பட்ட இரசாயன பாதியாகும்.
புதிய மருந்து அளவு படிவம்(NDF)
இலங்கையில் கிடைக்கக்கூடிய பதிவு செய்யப்பட்ட வடிவங்களைத் தவிர்த்து ஏனைய பதிவுசெய்யப்பட்ட எந்த ஒரு பௌதிக வடிவத்திலான மருந்து
புதிய இணைப்பு உற்பத்தி (NCP)
இலங்கையில் முன்னர் பதிவு செய்யப்படாத ஒரு தனி மருந்து அளவில் வடிவமைக்கப்பட்டுள்ள இரண்டு அல்லது அதற்கு மேற்பட்ட மருந்துகளின் ஒரு புதிய இணைப்பு உற்பத்தி
புதிய உற்பத்தி
இலங்கையில் ஏற்கனவே பதிவு செய்யப்பட்ட மருந்துகளின் ஏதேனும் புதிய உற்பத்தி
உயிரியல்சார்ந்த உற்பத்திகள்
தடுப்பூசிகளும் ஊநீரும் (Guidelines for Handling and Storage of Vaccines in the Private Sector)
Plasma products
Bio-technological products
Other biological products
சந்தைப்படுத்தும் அதிகாரத்திற்காக விண்ணப்பிக்கின்ற விண்ணப்பதாரி (உதா: உள்ளூர் தயாரிப்பாளர் அல்லது தயாரிப்பாளரை பிரதிநிதித்துவப்படுத்துகின்ற உள்ளூர் இறக்குமதியாளர்) அட்டவணை IVஇல் கொடுக்கப்பட்டுள்ள CDD ஒழுங்குவிதிகளின் A படிவத்தில், மருந்து மாதிரிகளுடன் ஒரு விண்ணப்பத்தை (தேவைப்படும் ஆவணங்கள்) தேசிய மருந்துகள் ஒழுங்குமுறைப்படுத்தும் அதிகாரசபைக்கு (NMRA) சமர்ப்பிக்க வேண்டும். விண்ணப்பத்தை சமர்ப்பிப்பதற்கு முன்னர் பதிவுசெய்யும் மாதிரிகளை இறக்குமதி செய்கின்றபோது சுங்கத் தடைகளை நீக்கிக்கொள்ளுவதற்கு வசதிசெய்துகொடுப்பதற்காக தேசிய மருந்துகள் ஒழுங்குமுறைப்படுத்தும் அதிகாரசபையிடமிருந்து (NMRA) பெற்றுக்கொண்ட மாதிரி அனுமதிப்பத்திரம் தேவைப்படுகிறது
Guidelines on Evaluation of Similar Bio therapeutic Products (SBPs)
மாதிரி இறக்குமதி அனுமதிப்பத்திரத்தைப் பெற்றுக்கொள்ளுதல்
இலங்கையில் சந்தைப்படுத்த கருதுகின்ற மருந்திற்கு அதிகாரம் கோரும் விண்ணப்பத்தை அனுப்பும்போது அந்த விண்ணப்பத்துடன் சந்தைப்படுத்தலுக்கு அதிகாரம் கோரும் மருந்தின் குறைந்த பட்சம் இரண்டு விற்பனை பொதிகளை சமர்ப்பிக்க வேண்டும். தயாரிப்பாளர் வெளிநாட்டவராக இருந்தால் பதிவு செய்யப்பட்ட அத்தகைய மாதிரிகளை இறக்குமதி செய்கின்றபோது சுங்க இசைவைப் பெற்றுக்கொள்ளுவதற்கு வசதிப்படுத்துவதற்காக தேசிய மருந்துகள் ஒழுங்குமுறைப்படுத்தும் அதிகாரசபையின் (NMRA) மாதிரி அனுமதிப்பத்திரம் தேவைப்படும்
பதிவுசெய்யப்பட்ட மாதிரிகளை இறக்குமதிசெய்வதற்காக விண்ணப்பதாரர் பின்வரும் ஆவணங்களை விண்ணப்பத்துடன் (அட்டவணை XI) சமர்ப்பிக்க வேண்டும்.
- விண்ணப்பதாரர் சமர்ப்பிக்கும் மாதிரி அனுமதிப்பத்திரத்திற்கான கோரிக்கை கடிதம்
- விண்ணப்பதாரர் தனது உள்ளூர் முகவர் என்பதைக் குறிக்கும் தயாரிப்பாளரின் அதிகார கடிதம்.
- தேசிய மருந்துகள் ஒழுங்குமுறைப்படுத்தும் அதிகாரசபையினால் (NMRA) வழங்கப்படும் மருந்துகள் தயாரிப்பு அமைவிடத்தற்கான அனுமதி கடிதம் (CP அனுமதி கடிதம்)
ஒரு குறித்த உற்பத்திக்கு மாதிரி அனுமதிப்பத்திரத்தை வழங்குவதை மறுக்கும் அதிகாரத்தை தேசிய மருந்துகள் ஒழுங்குமுறைப்படுத்தும் அதிகாரசபை (NMRA) கொண்டுள்ளது.
குறித்த பொருளின் பதிவுசெய்யப்பபட்ட உற்பத்திகள் இருபது அல்லது அதற்கு மேல் இருந்தால் தேசிய மருந்துகள் ஒழுங்குமுறைப்படுத்தும் அதிகாரசபை (NMRA) தற்பொழுது விண்ணப்பங்களை ஏற்றுக்கொள்ளாது.
Import of registration samples
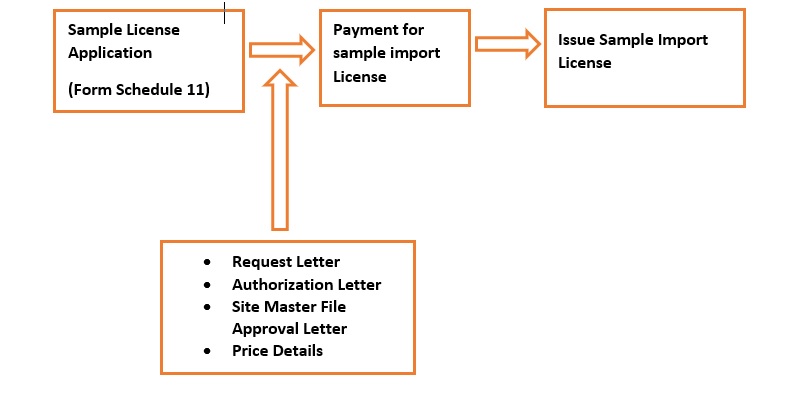
Submission of Registration Application
Figure 1: Registration of NP Applications
பதிவுச் சான்றிதழ் 5 வருடங்களுக்கு செல்லுபடியாகும். குறிப்பிட்ட சில சந்தர்ப்பங்களில் (உதா: மருந்து புதிய இரசாயன தனிபண்புளைக் கொண்டிருக்கும்போது, தயாரிப்பாளர் இந்த நாட்டுக்கு புதியவராக இருக்கும்போது) முதலில் ஒரு மாகாண பதிவு சான்றிதழ் வழங்கப்படும். அது ஒன்று அல்லது இரண்டு வருடங்களுக்கு செல்லுபடியானதாகும்.
நடைமுறையில் உள்ள பதிவு காலாவதியாவதற்கு 6 மாதங்களுக்கு முன் புதுப்பித்தல் விண்ணப்பமும் ஏனைய தேவைப்படும் ஆவணங்களும் அட்டவணை IV படிவம் Aயில் சமர்ப்பிக்கப்பட வேண்டும்.
பதியுசெய்யப்பட்ட மருந்தொன்றில் ஏற்படுத்தும் ஏதேனும் மாற்றங்கள் (வேறுபாடுகள்) NMRA, NME, NDF, NCP என்பவற்றிற்கு அறிவிக்கப்படுதல் வேண்டும்.
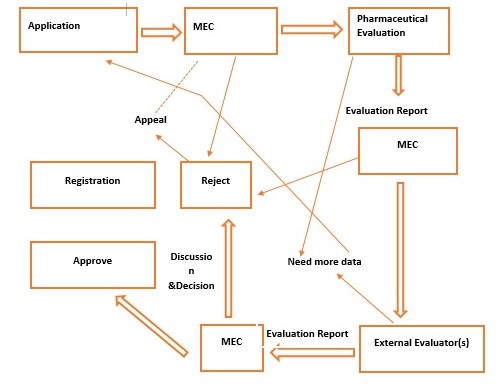
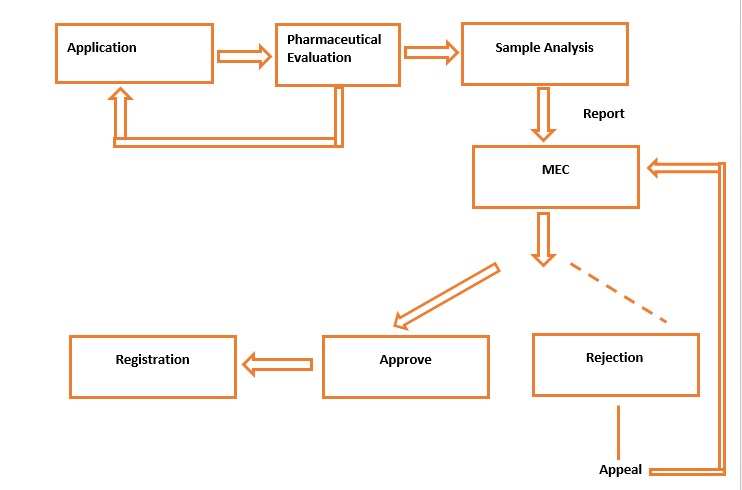
படம்2: NME, NDF, NCP என்பவற்றின் பதிவு